Epigenética Revela Vulnerabilidade Celular em Câncer Cerebral Infantil Agressivo
Nova análise aprofunda como alterações genéticas "sequestram" o desenvolvimento cerebral normal para iniciar tumores pediátricos, abrindo portas para terapias mais eficazes.
 Reprodução
Reprodução
A pesquisa em oncologia pediátrica frequentemente se depara com a complexidade de tumores cerebrais agressivos, como o ependimoma, o terceiro mais comum em crianças. Diferente de muitos cânceres em adultos, que exibem um grande número de mutações genéticas, os tumores pediátricos frequentemente possuem genomas "silenciosos", com poucas alterações genéticas recorrentes, mas com perfis epigenômicos profundamente alterados. Essa distinção sempre levantou um desafio fundamental: como, então, esses tumores se iniciam e progridem com tamanha agressividade? Uma nova análise publicada na Nature Medicine oferece uma resposta revolucionária, desvendando o "porquê" por trás da especificidade do ependimoma pediátrico.
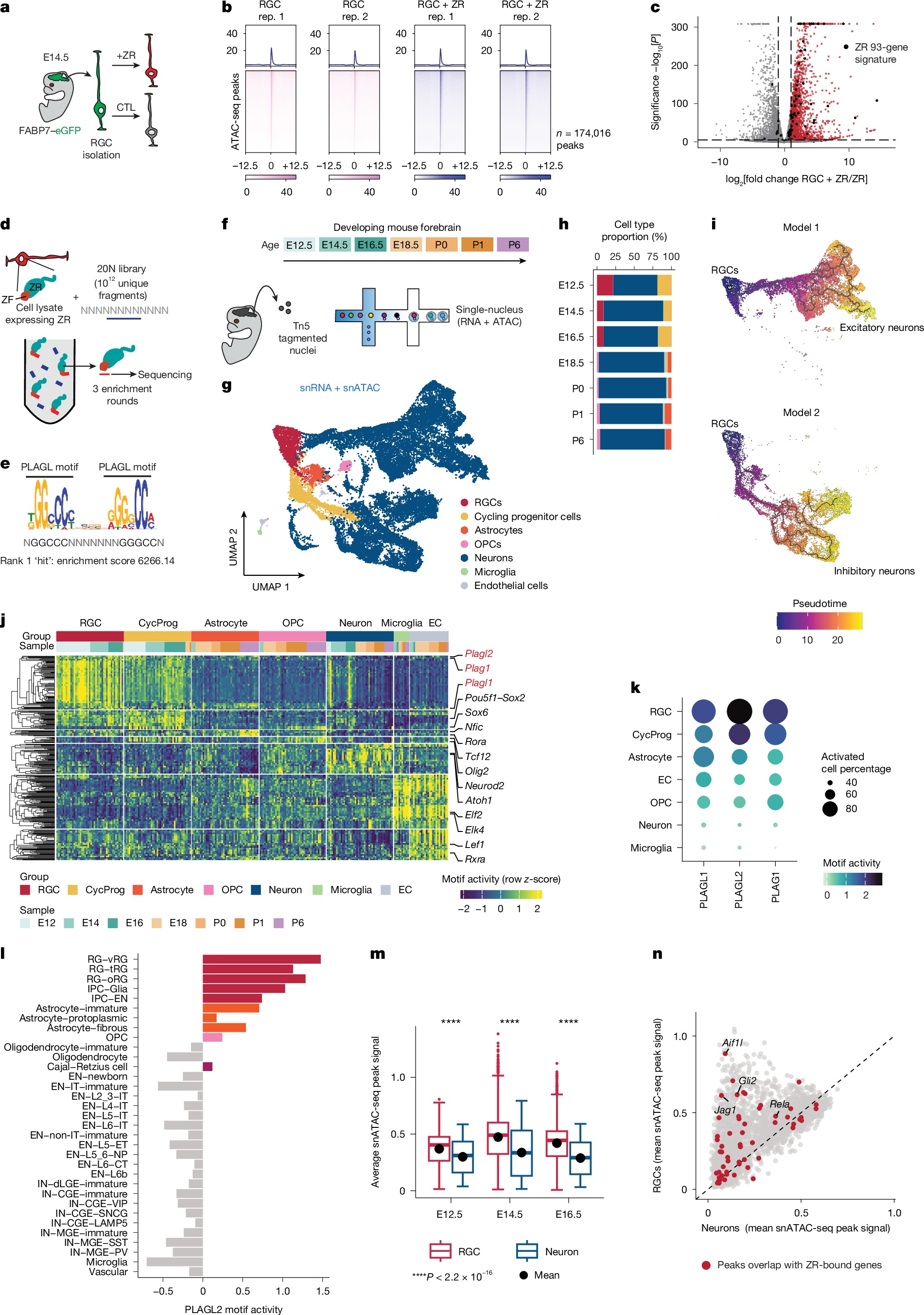
O cerne dessa compreensão reside na fusão oncoproteica ZFTA–RELA (ZR), identificada como a alteração genética mais recorrente no ependimoma supratentorial pediátrico. Contrariando a expectativa de que o ZR criaria um novo cenário epigenético para impulsionar o câncer, os pesquisadores descobriram algo muito mais insidioso: o ZR não remodela dramaticamente a acessibilidade da cromatina, mas sim "sequestra" estados epigenômicos já estabelecidos durante o desenvolvimento cerebral normal. Em outras palavras, ele não constrói um novo caminho, mas desvia um existente.
Essa descoberta é crucial porque explica por que o ependimoma impulsionado pelo ZR ocorre quase exclusivamente na infância e em regiões cerebrais específicas. Durante o desenvolvimento embrionário, certas células progenitoras transitórias possuem "módulos de cromatina" específicos, regulados por fatores de transcrição da família PLAG/L, que são naturalmente acessíveis. A oncoproteína ZR liga-se precisamente a esses módulos pré-existentes, induzindo a expressão de oncogenes e perpetuando um programa neoplásico. É um aproveitamento perverso de um processo biológico natural.
O impacto dessa revelação transcende a mera descrição do mecanismo. Ela transforma nossa visão sobre a iniciação e progressão de diversos cânceres pediátricos. Não se trata apenas de identificar uma mutação, mas de compreender "como" essa mutação "hackeia" o delicado processo de desenvolvimento. Para o leitor, isso significa que a porta se abre para estratégias terapêuticas inteiramente novas. Em vez de focar apenas em eliminar células tumorais, poderíamos desenvolver abordagens que impeçam esse sequestro epigenético, protegendo as células progenitoras ou reprogramando-as antes que se tornem malignas. A capacidade de identificar esses estados epigenômicos vulneráveis pode levar a biomarcadores para detecção precoce e tratamentos personalizados, oferecendo esperança real na luta contra um dos cânceres infantis mais desafiadores. Este é um salto paradigmático que nos aproxima de um futuro onde o tratamento do câncer pediátrico é menos invasivo e mais eficaz, mirando na raiz do problema.
Por que isso importa?
Contexto Rápido
- Cânceres pediátricos são caracterizados por genomas 'silenciosos' e menos mutações que suas contrapartes adultas, com aberrações epigenômicas desempenhando papel predominante.
- Ependimoma é o terceiro tumor cerebral mais comum em crianças, sendo agressivo e quimiorresistente.
- Oncoproteínas de fusão, como ZFTA–RELA, são drivers comuns de cânceres pediátricos e definem subtipos da doença, mas o mecanismo de como operam no contexto do desenvolvimento era incompletamente compreendido.